Nitrit: Revizyonlar arasındaki fark
Görünüm
| [kontrol edilmiş revizyon] | [kontrol edilmiş revizyon] |
İçerik silindi İçerik eklendi
Otorite kontrolü şablonu eklendi |
k →top: dz., ; Görünmez karakterler fark edilebilir kılındı: kırılmaz boşluk (U+00A0) |
||
| 105. satır: | 105. satır: | ||
|- |
|- |
||
|Molar kütle |
|Molar kütle |
||
|46.005 |
|46.005 g·mol <sup>−1</sup> |
||
|- |
|- |
||
|Eşlenik asit |
|Eşlenik asit |
||
Sayfanın 21.23, 21 Mart 2024 tarihindeki hâli
Bu madde hiçbir kaynak içermemektedir. (Temmuz 2022) (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |

| |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
dioxidonitrate(1−) | |||
Diğer adlar nitrite | |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| EC Numarası |
| ||
PubChem CID
|
|||
| UNII | |||
| |||
| |||
| Özellikler | |||
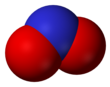
| Kimyasal formül | NO2 | ||
| Molekül kütlesi | 46,01 g mol−1 | ||
| Konjuge asit | Azotlu asit | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||
Nitrit iyonu kimyasal formül NO'ya sahiptir .-
2. Nitrit (çoğunlukla sodyum nitrit ), kimya ve ilaç endüstrilerinde yaygın olarak kullanılmaktadır. Nitrit anyonu, doğada azot döngüsünde yaygın bir ara maddedir . Nitrit adı, nitröz asidin esterleri olan – ONO grubuna sahip organik bileşiklere de atıfta bulunabilir .